クロム 銅 電子配置
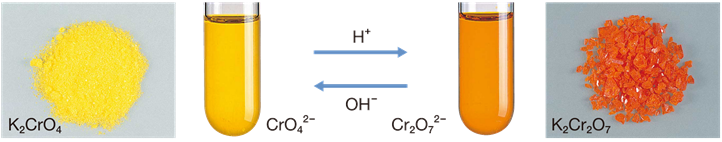
クロムCr原子の電子配置 代表的なものにクロム酸カリウム K 2 CrO 4 や二クロム酸カリウム K 2 Cr 2 O 7 があり,これらの6価化合物は有毒です。 K 2 CrO 4 の黄色水溶液に酸を加えると K 2 Cr 2 O 7 が生じて橙赤色になり,逆に K 2 Cr 2 O 7 の溶液に塩基を加えると K 2 CrO.

クロム 銅 電子配置. 酸化クロム 5種類が存在する。 酸化クロム(ii)(cro) 酸化クロムの1種。 酸化クロム(iii)(cr 2 o 3 ) 同上。 酸化クロム(vi)(cro 3 ) 同上。 クロム酸カリウム(k 2 cro 4 ) 6価の化合物で、強力な酸化剤。 劇物として扱われ、6価クロムによる汚染の際、問題になることも多い。. もうひとつは、銅の価数と電子の入り方についてです。 電子の入り方のルールを自分なりに理解して、 銅とクロムの電子の入り方をノートにまとめていた時に思ったことがあります。 銅の電子の入り方です。. 遷移元素のイオン化エネルギーは、約 550 ~ 900 kJ/mol の間です。 これは、リチウム Li やストロンチウム Sr から、ホウ素 B やリン P までの範囲に相当します。 このことは、遷移元素の作る結合が、イオン結合性から共有結合性まで、多様であることを示しています。.
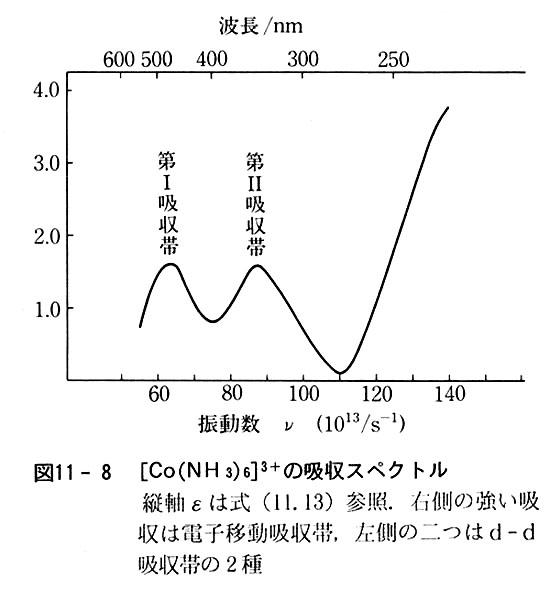
Ti3の基底電子配置は3d1なの でT に電子が1つ入っている 6 液の電子吸収スペクトル 2g . この電子がdd遷移を起こす. 授業内容 1回元素と周期表・量子力学の起源 2回古典力学の破綻・波と粒子の二重性 3回シュレディンガー方程式・波動関数のボルンの解釈. 電子配置 基底状態の電子配置表 (第1 第7周期)族元素記号原子番号KLMNOPQ最大電子数第1周期1s2s2p3s3p3d4s4p4d4. 問題16:無機化学における異性現象 <解答> 1 Ar3d6.3d 軌道の中の電子配置は下図のようである. 2 Co(NH 3) 6 3及びCoF 6 3は,NH3 及びFからCo(III)への非共有電子対の供与によって配位結合し,それぞれ内軌道錯体及び外軌道錯体を形成する.そのため,それぞれの錯体の電.
化学 電子配置について クロムや銅で、N殻からM殻へ電子が1つ移動するのは、なぜですか? また、(高校)授業で、この配置の規則を覚えれば、原子番号37番以降についても電子配置を求められる、と習ったのですが、37番以降も、クロムや銅のように6族、11族の最外殻電子が、1つ減るという. 電子配置を軌道により組み分けする:1s 2s2p 3s3p 3d 4s4p 4d 4f 5s5p 5d 5f ・・・すなわち,主量子数nで にくくるのであるが、その中でd, f 電子は別扱いとする.いま,主量 子数nにある電子の遮蔽定数δを求めることを考えよう.この電子より. の電子配置が変化していくs,pブロック元素 →典型元素と呼ばれる 最外殻の電子数が変わるので,原子番号が1つ増えると 化学的性質が大きく変化する. 一方,周期を縦にずれても最外殻の軌道が似ているので ・結合を何本作れるか.
個ずつ電子が収容されるまで,1個の軌道に1個ずつ電子が収容され る.このとき,これらの電子はすべてじ向きのスピンをもつ.(この規 則はすべての元素で成り立つわけではない) Ground state ↓ 原子の電子配置に関するルール 無機化学導入講義. 2 有機銅錯体(organocuprate) の合成(H Gilman) ・4s/3d, 5s/4d, 6s/5d軌道のエネルギーが近く複雑な電子配置を取るため、大小関係がまちまち 相対論効果 重元素では、1s電子の速度vが増加する(式1)。 電子質量の増加(式2) とBohr半径の減少(式3)。. の電子配置が変化していくs,pブロック元素 →典型元素と呼ばれる 最外殻の電子数が変わるので,原子番号が1つ増えると 化学的性質が大きく変化する. 一方,周期を縦にずれても最外殻の軌道が似ているので ・結合を何本作れるか.
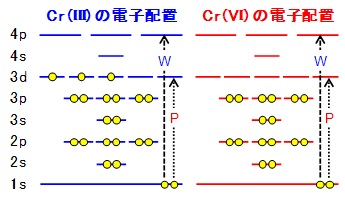
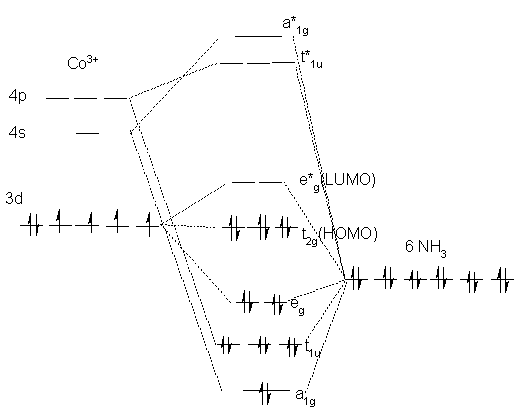
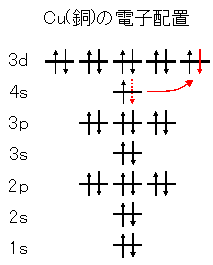
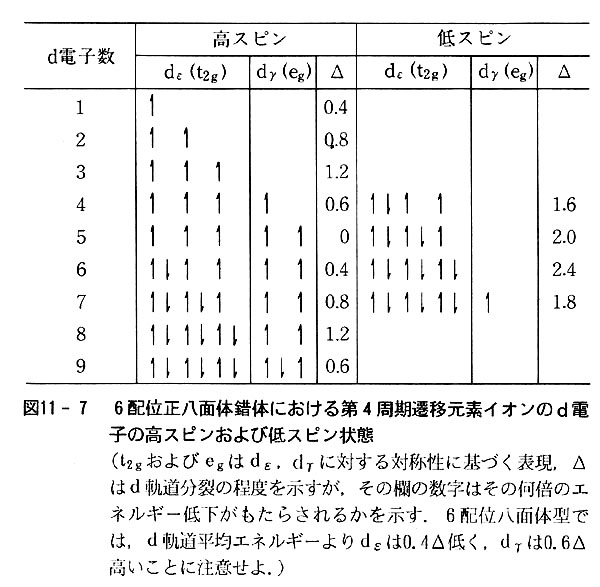
八面体形錯体ではd1~d3及びd8~d9では電子の占め方が一通 りであるが,d4~d7では二通りの電子配置がある。不対電子の数が多くなる方を高スピン配置(HighSpin Configuration), 少なくなる方を 低スピン配置 (LowSpin Configuration)という。. 明し,電子遷移に伴う金属錯体の色について解説する。 金属錯体の形と色 YAMAGUCHI Yoshitaka 山口 佳隆 横浜国立大学大学院工学研究院 教授 図2 s軌道とp軌道の形 図3 酸素の電子配置と仮想的な水分子 図4 炭素の電子配置とsp 3混成による四面体構造. これはクロム(原子番号24)と銅(原子番号29)の原子の電子配置(Cr;1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 5 、Cu;1s 2 2s 2 2p 6 3s 2 3p 6 4s 1 3d 10 )のところで出て来た不規則性に関係があります。4s軌道と3d軌道の順番は原則的には4s<3dですが、そのエネルギー差は小さい.
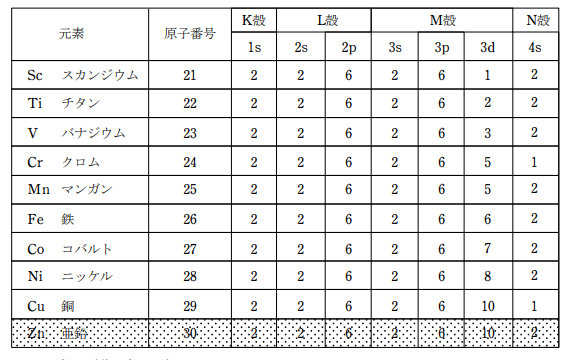
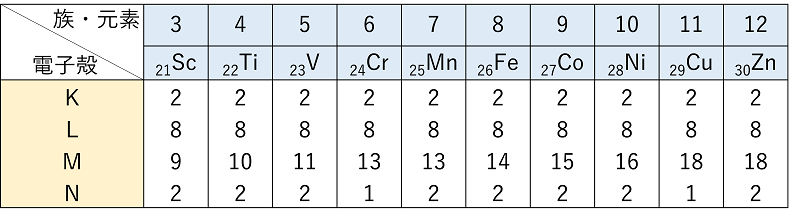
2 銅の電子配置と 銅イオンの電子配置を教えてください 3 化学 銅Cuについて Cuは原子番号29 で最外殻に一つの価電子をもっていますがなぜCu「2」のイ 4 高1化学基礎の問題です。 銅Cu(64)を燃焼させ酸化銅CuO(80)にした。 銅192gを全て酸. 酸化クロム 5種類が存在する。 酸化クロム(ii)(cro) 酸化クロムの1種。 酸化クロム(iii)(cr 2 o 3 ) 同上。 酸化クロム(vi)(cro 3 ) 同上。 クロム酸カリウム(k 2 cro 4 ) 6価の化合物で、強力な酸化剤。 劇物として扱われ、6価クロムによる汚染の際、問題になることも多い。. 図1 カリウムから亜鉛までの電子配置(閉殻の部分は省略) 赤く強調されているクロム(Cr)と銅(Cu)はよく見ると、ほかと少し違う電子配置になっている。 4s軌道から3d軌道に電子が1個移っている のである。 どうしてこのようなことをする必要があるのだろうか。.
メモ: →内容変更:銅のイオンの価数のビデオを視聴してまとめる 4/21(土)の行動計画 項目: 昨日の復習+昨日見た銅の電子配置に関する資料をまとめておく 目標: 1h 項目: 橋元・物理基礎(1) 目標: 2h30m. 電子配置一覧表 プロ講師解説このページでは『原子番号1〜36までの元素の電子配置』を一覧表でまとめました。 (電子を並べる際のルールやその他電子配置に関する基本事項については 図解電子配置とは?. 遷移元素のイオン化エネルギーは、約 550 ~ 900 kJ/mol の間です。 これは、リチウム Li やストロンチウム Sr から、ホウ素 B やリン P までの範囲に相当します。 このことは、遷移元素の作る結合が、イオン結合性から共有結合性まで、多様であることを示しています。.
メモ: →内容変更:銅のイオンの価数のビデオを視聴してまとめる 4/21(土)の行動計画 項目: 昨日の復習+昨日見た銅の電子配置に関する資料をまとめておく 目標: 1h 項目: 橋元・物理基礎(1) 目標: 2h30m. Accepted for publication December 3, 19;. 2 銅の電子配置と 銅イオンの電子配置を教えてください 3 化学 銅Cuについて Cuは原子番号29 で最外殻に一つの価電子をもっていますがなぜCu「2」のイ 4 高1化学基礎の問題です。 銅Cu(64)を燃焼させ酸化銅CuO(80)にした。 銅192gを全て酸.
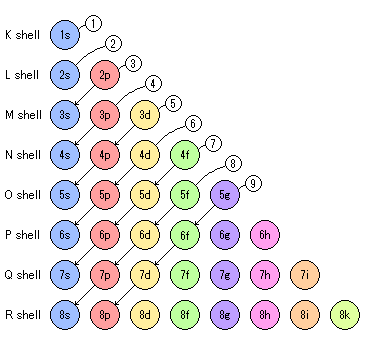
原子番号原子番号Zの原子の電子配置が決まっているとき、 原子番号 Z1の原子については、新たにつけ加わる 1個の電子に、空いている軌道のうち エネルギエネルギ の ー の 最も低い軌道の量子数 を割り当てる。 1s < 2s < 2p < 3s < 3p < 4s < 3d < 4p < 5s < 4d < 5p < 6s. 錯体の多電子配置のエネルギー準位を考える Coordination Chemistry 2D E elec >E LF 電子間反発によ るエネルギー分 裂のみを考える 配位子場に よるエネル ギー分裂の みを考える 例えばd1 (E elecはないがわかりやすいので) 2T 2g 2E g E elec only E elec <E LF 弱配位子場. 2 銅はCu2のほうがCuより安定です。 銀に比べて異常なこの現象には2つの理由が考えられます。 ① 銅の3d軌道は銀の4d軌道に比べて原子核に近く軌道が小さいので10個の3d電子で閉殻になると電子間反発が閉殻の安定化効果を上回るのです。.
問題16:無機化学における異性現象 <解答> 1 Ar3d6.3d 軌道の中の電子配置は下図のようである. 2 Co(NH 3) 6 3及びCoF 6 3は,NH3 及びFからCo(III)への非共有電子対の供与によって配位結合し,それぞれ内軌道錯体及び外軌道錯体を形成する.そのため,それぞれの錯体の電. ページの上に戻る ©0121 NetAdvance Inc All rights reserved. ピン状態の電子配置がある.高スピン状態では電子はt2g, eg軌道の順に一つずつ電子が埋まっていく. 低スピン状態では,電子はまず,t2g 軌道を完全に埋めてからエネルギー状態の高い eg 軌道を埋めてい く..
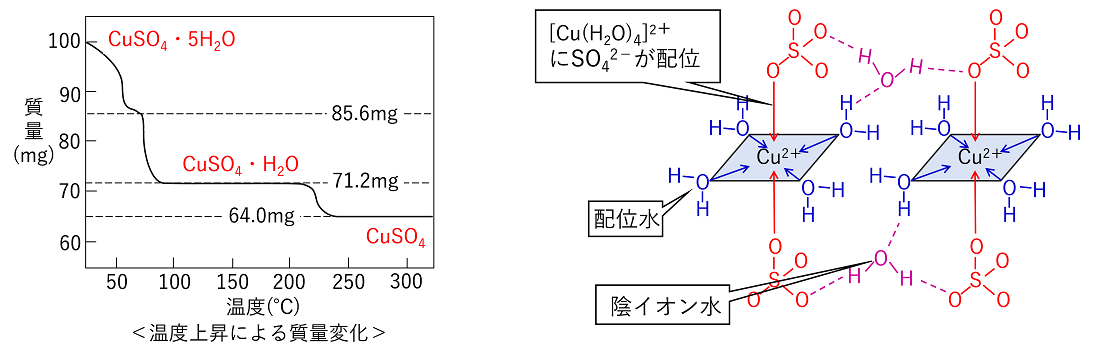
2 銅はCu2のほうがCuより安定です。 銀に比べて異常なこの現象には2つの理由が考えられます。 ① 銅の3d軌道は銀の4d軌道に比べて原子核に近く軌道が小さいので10個の3d電子で閉殻になると電子間反発が閉殻の安定化効果を上回るのです。. 2 有機銅錯体(organocuprate) の合成(H Gilman) ・4s/3d, 5s/4d, 6s/5d軌道のエネルギーが近く複雑な電子配置を取るため、大小関係がまちまち 相対論効果 重元素では、1s電子の速度vが増加する(式1)。 電子質量の増加(式2) とBohr半径の減少(式3)。. A14 ハイライト 電子を描く(10) ― 元素の周期表を原子軌道で描く 時田 澄男a*,時田 那珂子b a埼玉大学名誉教授,〒 さいたま市桜区下大久保255 bSTUDIO NEBULA, 〒 さいたま市浦和区神明179 *email tokita@apcsaitamauacjp (Received November 22, 19;.
化学 Crの軌道について 今、学校で物理化学の勉強をしていてよく分からない点があったので質問します。 クロムの軌道で、クロムは電子を24個もっているので、1s軌道~4s軌道は満杯になり、3d軌道に 質問No.

電子配置一覧表 化学のグルメ
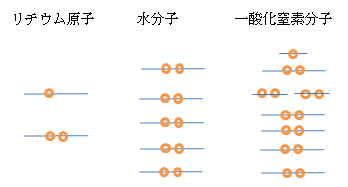
驚きの電子配置をもつ高効率発光材料
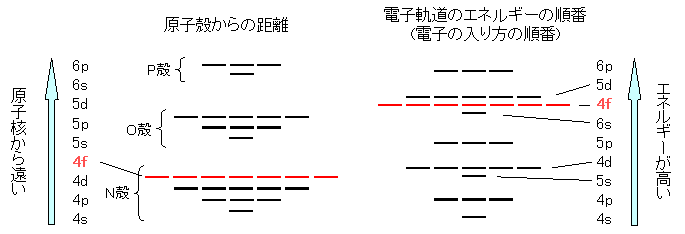
研究解説 希土類元素の物理化学 その2
クロム 銅 電子配置 のギャラリー

研究解説 希土類元素の物理化学 その2

キリヤ Q A
基底状態における銅の電子配置は という問題を解きたいです この問題の答 Yahoo 知恵袋
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo Coordination chemistry part2 Pdf

金属錯体の色や磁気的な性質
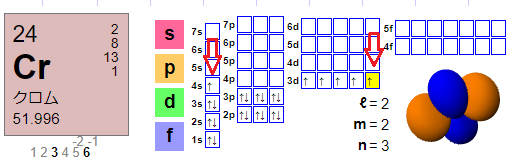
電子配置から考える Trans To Trans
Cu とcu 2の違いを教えてください それぞれの電子配置図を交えて説明 Yahoo 知恵袋

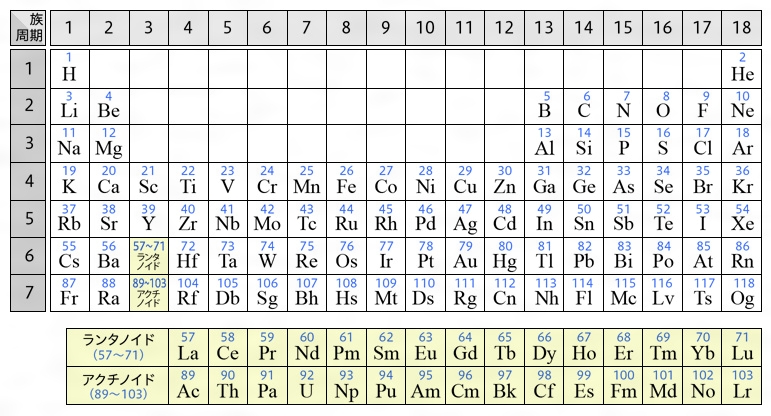
周期表 Wikipedia
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo Coordination chemistry part2 Pdf

大学無機化学 電子配置 クロムや銅の電子配置は Youtube

多電子原子の電子配置 2 Dブロック元素
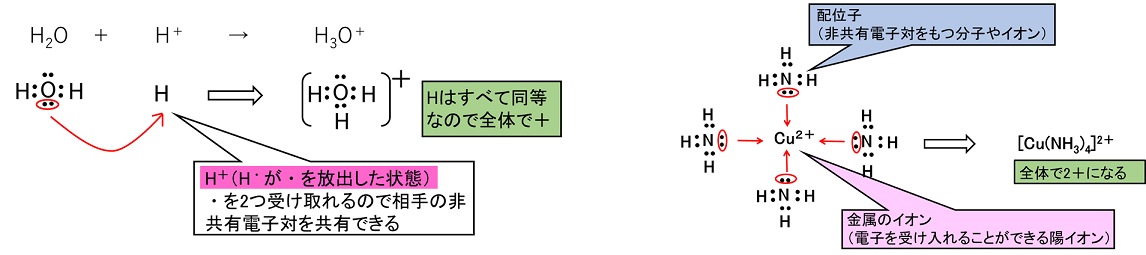
遷移元素の特色

Grain3 孤独な電子と浮かれる電子 With Ferrite By Tdk Tdk Techno Magazine
基本知識ですみません クロムの基底状態の電子配置です 電子の埋 Yahoo 知恵袋
Q Tbn And9gctfynqgxlk1gm61nvjqil0wvfewnnf Pauqdjims Lupzdquv3w Usqp Cau
元素の電子配置について ネットで調べてると1s2s2p3s3pの Yahoo 知恵袋
なぜcrの電子配置は3d 44s 2ではなく3d 54sとなるのですか Yahoo 知恵袋

語呂合わせと徹底整理で攻略する高校無機化学 遷移元素と錯イオン篇 永野裕之のblog
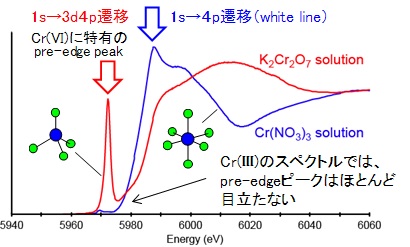
研究解説 Xafs その2

多電子原子の電子配置 2 Dブロック元素

化学基礎 電子配列の問題です 化学に関する質問 勉強質問サイト

遷移元素の特色

金属錯体の色や磁気的な性質
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo Coordination chemistry part2 Pdf

遷移元素の価電子の謎 大学の化学が分かる バラエティーゆたか

銅イオンは2価が安定な理由 日々の雑記帳
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo E8 87 E6 96 99 Ef 95 E7 84 A1 E6 9f E5 8c 96 E5 Ad A65 Pdf
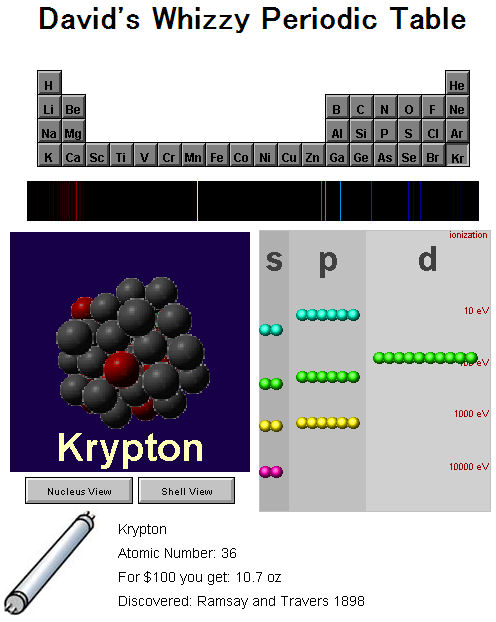
坂根弦太のdv Xa Venus日誌
Sp軌道 化学 画像の問3で Crの場合 なぜ4sに1個 3dに5個 Yahoo 知恵袋
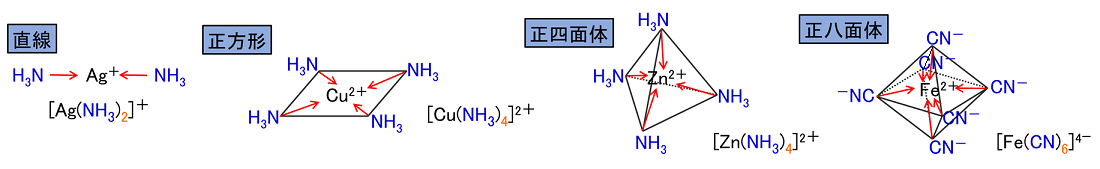
遷移元素の特色
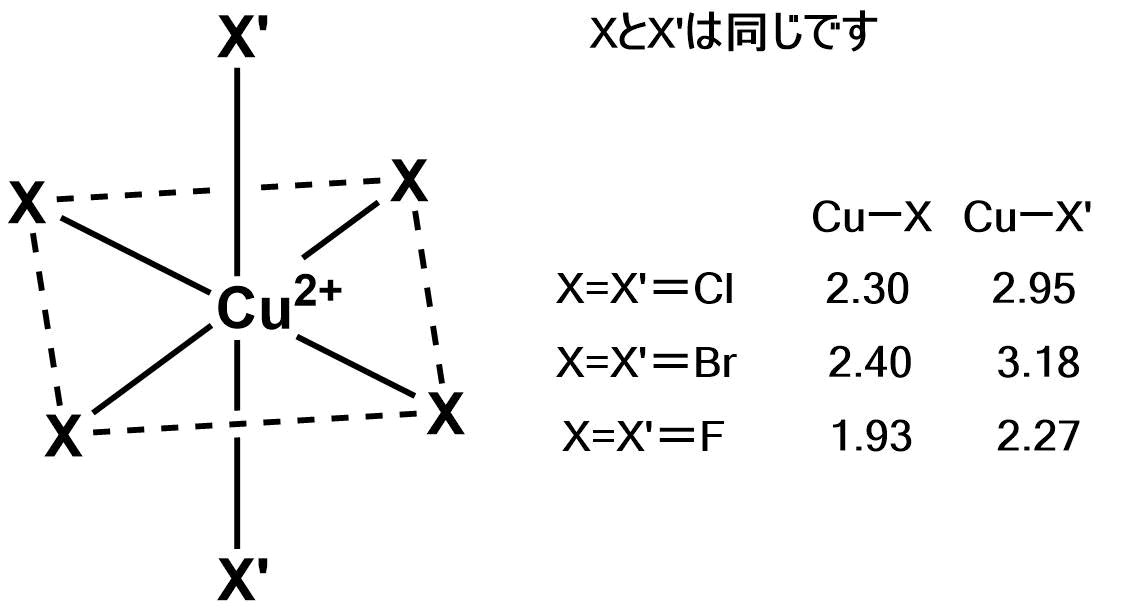
ヤーン テラー効果

構造原理 Aufbau Principle カタギリノエンレイソウ広報
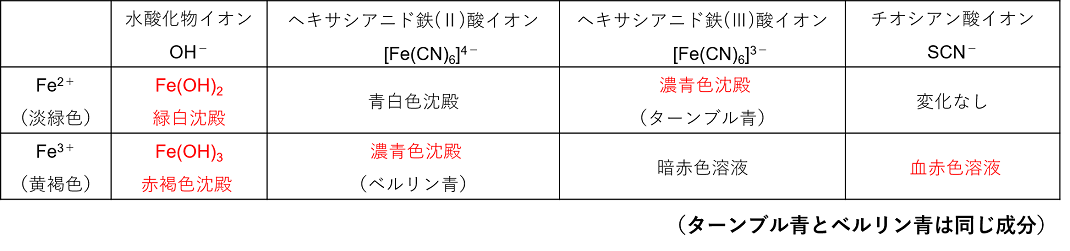
無機化学 第11回 遷移元素 Fe 医学部受験を決めたら 私立 国公立大学医学部に入ろう ドットコム

研究解説 希土類元素の物理化学 その2

構造原理 Aufbau Principle カタギリノエンレイソウ広報

多電子原子の電子配置 2 Dブロック元素
研究解説 Xafs その2

原子の電子配置 第4周期まで と電子軌道のエネルギー準位 Irohabook

銅 Wikipedia

レビトロンゼロ
電子配置一覧表 化学のグルメ

Periodic Table Cr
銅 Wikipedia

4 です 私の答え 希ガスであり 電子配置が安定してい 化学に関する質問 勉強質問サイト

2 なぜ銅の参加数は 2なのか 金属は電子を1つ放出して1 化学に関する質問 勉強質問サイト
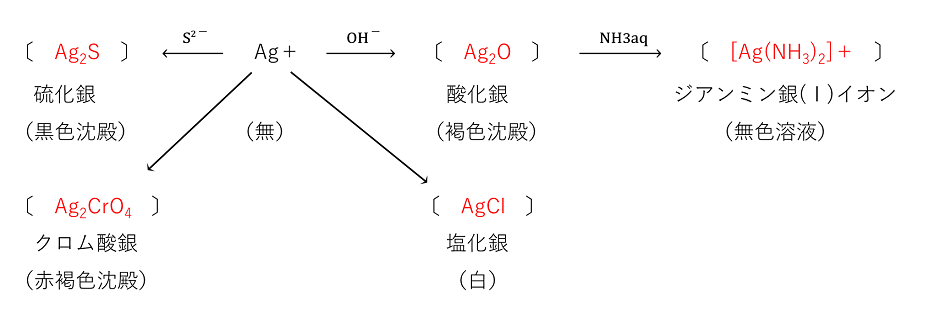
無機化学 錯イオン生成反応
イオン式とは 価数とは 書き方や語呂合わせの覚え方 暗記法まとめ 高校化学の問題の解き方も 受験の相談所
Q Tbn And9gctfynqgxlk1gm61nvjqil0wvfewnnf Pauqdjims Lupzdquv3w Usqp Cau

けみけみケミストリー 大学無機化学第7回目の講義です 電子配置について解説しています 大学無機化学 電子配置 クロムや銅 の電子配置は T Co Rzopztaq5j
電子配置から考える Trans To Trans

Grain3 孤独な電子と浮かれる電子 With Ferrite By Tdk Tdk Techno Magazine
クロムの電子配置が K殻に2個 L殻に8個 M殻に13個 N殻に1 Yahoo 知恵袋

周期表の化学 日々の雑記帳

電子配置から考える Trans To Trans

キリヤ Q A

構造原理 Aufbau Principle カタギリノエンレイソウ広報
クロムとは コトバンク

キリヤ Q A

語呂合わせと徹底整理で攻略する高校無機化学 遷移元素と錯イオン篇 永野裕之のblog
Q Tbn And9gcrsdx3xymndzdmiraefdm 5cjbfmhtwiub2cqa6xnpg1eja0uax Usqp Cau

遷移元素 Wikipedia

化学分析屋さんの分析ノート 環境計量士 濃度関係 の過去問解説 環化 問6 19

電子配置
イオン化エネルギーと電子親和力
遷移元素の特色

2 なぜ銅の参加数は 2なのか 金属は電子を1つ放出して1 化学に関する質問 勉強質問サイト

Grain3 孤独な電子と浮かれる電子 With Ferrite By Tdk Tdk Techno Magazine

語呂合わせと徹底整理で攻略する高校無機化学 遷移元素と錯イオン篇 永野裕之のblog
遷移金属と金属錯体 理論編

電子配置から考える Trans To Trans
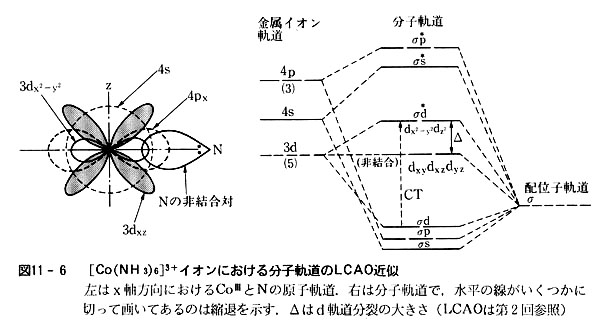
3 錯体の性質と配位結合

多電子原子の電子配置 2 Dブロック元素
遷移元素の特色

構造原理 Aufbau Principle カタギリノエンレイソウ広報

構造原理 Aufbau Principle カタギリノエンレイソウ広報
構造原理 Aufbau Principle カタギリノエンレイソウ広報
Http Www Lst Hokkai S U Ac Jp Kubo Pdf Chem4 Pdf

Cuが電子を失うとcu2 になる理由教えてください Clear
遷移元素の特色
研究解説 希土類元素の物理化学 その2

銅イオンの価数の謎 Trans To Trans
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo Coordination chemistry part2 Pdf

センイゲンソ 意味 読み方 使い方 英和 エキサイト辞書

電子配置
3 錯体の性質と配位結合
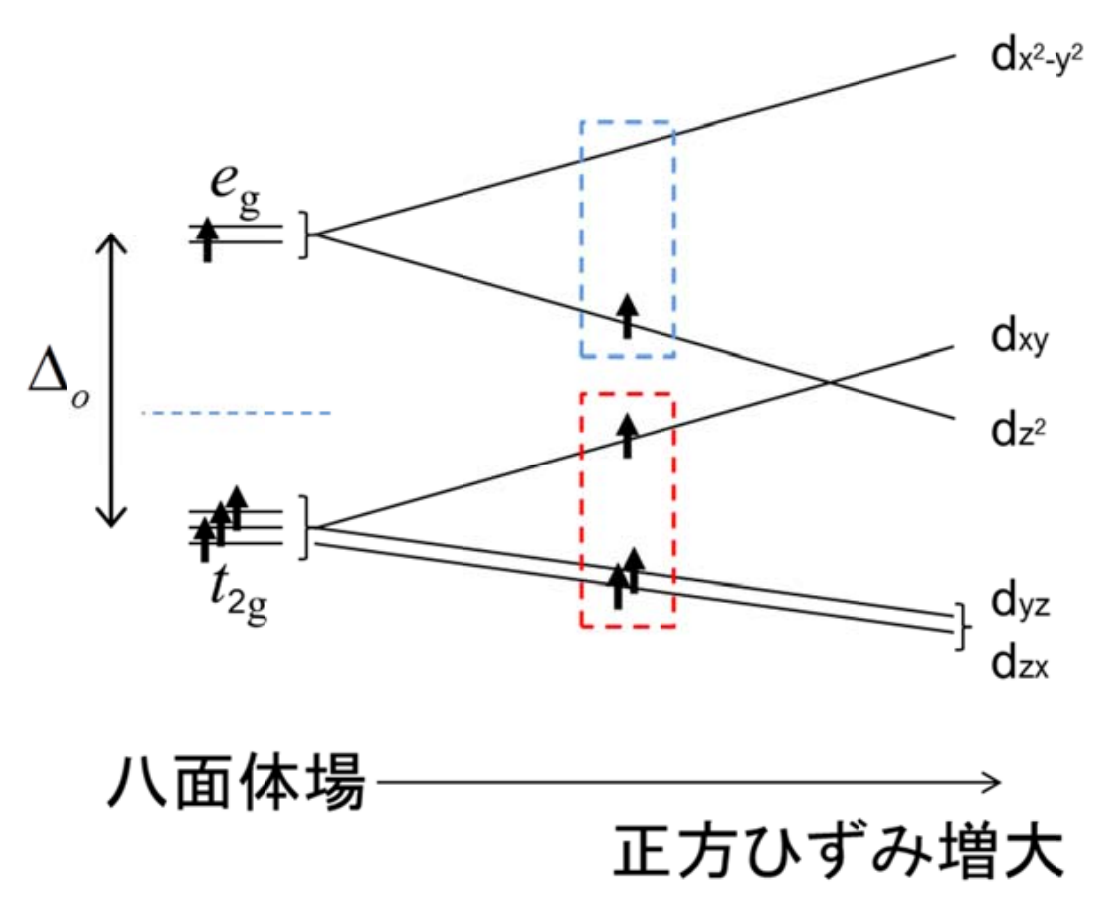
ヤーン テラー効果
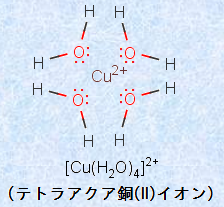
無機化学 錯イオン生成反応
遷移元素の特色

第4節 遷移金属とその化合物
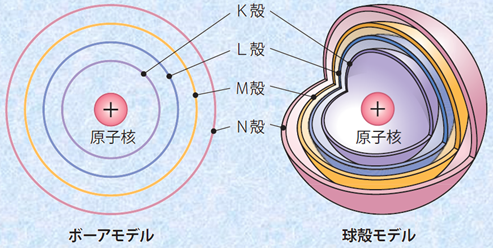
イオン化エネルギーと電子親和力

周期表の化学 日々の雑記帳

構造原理 Aufbau Principle カタギリノエンレイソウ広報

電子配置
Q Tbn And9gctqwddt5x0fscejx9c2lamnnxm60f7gsqppn6pcktuiaysggbmu Usqp Cau
3 錯体の性質と配位結合
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo E8 87 E6 96 99 Ef 95 E7 84 A1 E6 9f E5 8c 96 E5 Ad A65 Pdf

語呂合わせと徹底整理で攻略する高校無機化学 遷移元素と錯イオン篇 永野裕之のblog
Http Www Chem Nara Wu Ac Jp Tanase Classesinfo E8 87 E6 96 99 Ef 95 E7 84 A1 E6 9f E5 8c 96 E5 Ad A65 Pdf
Http Acbio2 Acbio U Fukui Ac Jp Phychem Maeda Kougi Bqc 12 02may12 Pdf
遷移元素 クロム マンガン 鉄 コバルト
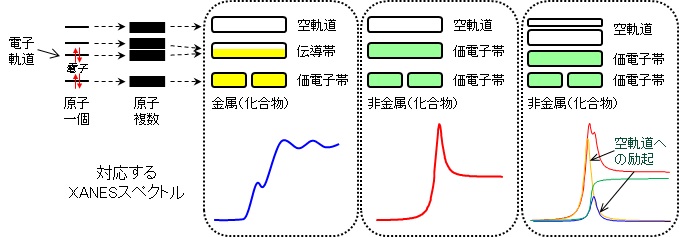
研究解説 Xafs その2




